| chemie-master.de: CD-ROM-Fassung bestellen |
Das Periodensystem der Elemente für den Schulgebrauch |
zurück |
| Technetium | |
(Mangangruppe) 5. Periode _______________ 7. Gruppe (IUPAC 89) |
|
|
|
|
| Elementart: Metall | Oxidationsstufe(n): +7 (+4, +5, +6) |
| Schmelztemperatur: 2157 °C (2430 K) | Elektronegativität: 1,9 |
| Siedetemperatur: 4265 °C (4538 K) | Atomradius: 135 pm |
| Dichte: 11,5 g/cm3 | Erdkrustenhäufigkeit: 5×10–16 % |
| Anordnung der Elektronen | |||||||||||||||||||
| 1s | 2s | 2p | 3s | 3p | 3d | 4s | 4p | 4d | 4f | 5s | 5p | 5d | 5f | .. | 6s | 6p | 6d | ... | 7s |
| 2 | 2 | 6 | 2 | 6 | 10 | 2 | 6 | 6 | 1 | ||||||||||
| Name | Von "technetos", griech. künstlich. | ||||||
| Entdeckung | Technetium wurde 1937 von Emilio Segré und Carlo Perrier (Rom) in kleinsten Mengen in einer Molybdänprobe gefunden. Diese hatte Ernest O. Lawrence im Cyclotron in Berkeley (USA) mehrere Monate lang mit Deuterium-Kernen bestrahlt und zur Analyse nach Italien geschickt. Segré und Perrier konnten aus dem mit Deuterium bestrahlten Molybdän eine radioaktive Fraktion abtrennen, die ungefähr ein zehnmillionstel Milligramm des bisher unbekannten radioaktiven Elements enthielt: 42Mo + D Technetium war damit das erste künstlich erzeugte Element, was auch in der Namensgebung für das neu gefundene Element seinen Niederschlag fand. 1952 gelang am Oak Ridge National Laboratory (USA) erstmals die Reindarstellung von metallischem Technetium durch Reduktion von Technetat mit Wasserstoff. |
||||||
| Eigenschaften | Silbergraues, radioaktives Schwermetall. Technetium ist unlöslich in Salzsäure, löslich in Salpetersäure und Königswasser sowie in konzentrierter Schwefelsäure. In seinem chemischen Verhalten ähnelt es mehr dem Rhenium als dem Mangan. Chlor greift das Metall kaum an. Mit Sauerstoff bildet sich Technetium(VII)-oxid Tc2O7. Von diesem Oxid, in dem Technetium mit der Oxidationsstufe +7 vorliegt, leiten sich die Pertechnetate, z.B. Natriumpertechnetat NaTcO4, ab. | ||||||
| Vorkommen | Das natürliche Vorkommen des Technetiums beschränkt sich auf geringste Spuren in Uranerzen. Es entsteht durch den Zerfall von 99Mo (Molybdän-99), einem Spaltprodukt des Urans. Das langlebige Isotop 99Tc wird als Spaltprodukt des Uran in Kernreaktoren gewonnen und steht heute in größerem Umfang zur Verfügung. |
||||||
| Verwendung | 99mTc ist die überwiegend verwendete Strahlungsquelle in der Nuklearmedizin (z.B. zur Szintigrafie von Schilddrüse oder Skelett).Szintigraphie mit Technetium-99m99Mo zerfällt mit einer Halbwertszeit von 66,02 Stunden in das metastabile 99mTc. Dabei wandelt sich ein Neutron unter Herausschleudern eines Elektrons in ein Proton um, so dass die Kernladungszahl Z um 1 ansteigt, die Massenzahl aber gleich bleibt. Aus Molybdän (Z = 42) wird also Technetium (Z = 43).99Mo (Kernreaktion im Generator) Der metastabile 99mTc-Kern muss noch Energie abgeben. Er zerfällt mit einer Halbwertszeit von 6,02 Stunden unter Aussendung von gamma-Strahlung in 99Tc. 99mTc (Für die Szintigraphie maßgebende Kernreaktion)  Generator zur Erzeugung von 99mTc aus 99Mo. (oben) und Funktionsmodell (unten).
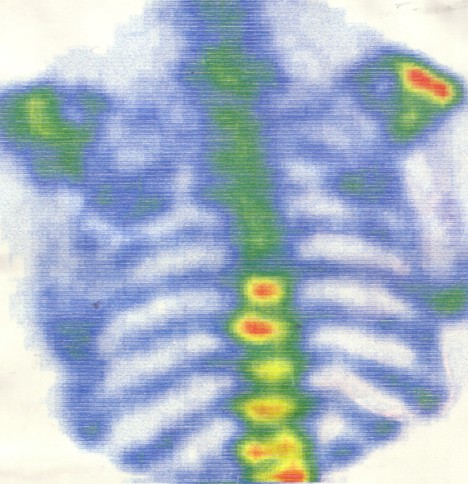 Die mit 99mTc markierte Lösung für Skelettuntersuchungen wird dem Patienten injiziert. Sie lagert sich speziell in Bereichen veränderten Knochenwachstums an. Mit Hilfe von Detektoren lässt sich die Gammastrahlung außerhalb des Körpers registrieren. Computerprogramme erstellen aus den Messwerten ein Bild des Skeletts. Das oben abgebildete Szintigramm zeigt Krebsmetastasen im Bereich des Schultergelenks und der Wirbelsäule.
Weitere Einsatzmöglichkeiten für Technetium sind:
|
||||||
| Isotope |  Nur Radionuklide, keine stabilen Isotope. Nur Radionuklide, keine stabilen Isotope.Bekannt sind Isotope von 85Tc bis 115Tc. Die Halbwertszeiten liegen zwischen Bruchteilen einer Millisekunde und 4,2 Millionen Jahren (bei 98Tc). Von Bedeutung sind: 99Tc (beta-Strahler, Halbwertszeit 2,11 × 105 Jahre) 99mTc (gamma-Strahler, Halbwertszeit 6,01 Std.) 95mTc (durch Elektroneneinfang entsteht 95Mo, Halbwertszeit 61 Tage). |
||||||
| Redox-Potenziale |
|
 |
© chemie-master.de - Website für den Chemieunterricht | Seitenübersicht| Lizenz & Urheberrecht| Arbeitsblätter | | Danksagungen | Kritik | Links | |
 |
| Quellenangabe für diese Seite: http://www.chemie-master.de/pse/pse.php?modul=Tc [Stand 10.06.2026] |
||
 |
||