| chemie-master.de: CD-ROM-Fassung bestellen |
Das Periodensystem der Elemente für den Schulgebrauch |
zurück |
 Metalle (Me) |
||
|
|
||
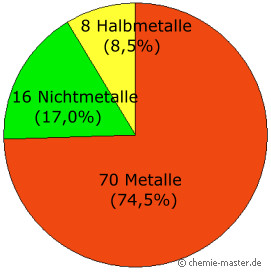
| Metalle | Die Abkürzung Me wird in Reaktionsgleichungen für ein beliebiges Metall verwendet. Es gibt kein Metall mit dem Symbol Me. Beispiel: Me + 2 H3O+ + 2 Cl– Metalle zeigen einen typischen Glanz. Sie sind allesamt elektrische Leiter und auch gute Wärmeleiter. Die Metalle und deren Legierungen kristallisieren in Form von Metallgittern. In einem solchen Gitter sind die Gitterpunkte durch positiv geladene Metallionen besetzt. Die abgespaltenen Außenelektronen bewegen sich zwischen den Metallionen umher und bewirken deren Zusammenhalt. Diese mehr oder weniger frei beweglichen Elektronen werden oft als »Elektronengas« bezeichnet. Sie sind die Träger der elektrischen Leitfähigkeit der Metalle. Siehe hierzu: Tabellen "Wärmeleitfähigkeit" bzw. "Elektrische Leitfähigkeit".
 Metallkugeln auf einem Brunnen (Fontaines de Bury, Palais Royal, Paris).
|
 |
© chemie-master.de - Website für den Chemieunterricht | Seitenübersicht| Lizenz & Urheberrecht| Arbeitsblätter | | Danksagungen | Kritik | Links | |
 |
| Quellenangabe für diese Seite: http://www.chemie-master.de/pse/pse.php?modul=metall [Stand 10.06.2026] |
||
 |
||