|
Lexikon "Fachbegriffe" |
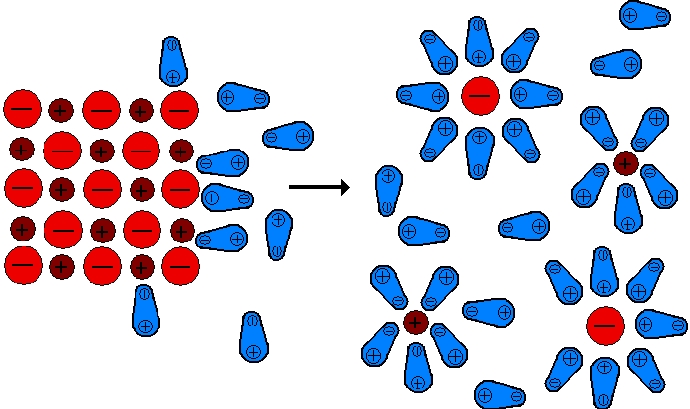
| In wässriger Lösung umgibt sich jedes Ion sofort mit einer Hydrathülle, die aus Dipol-Molekülen des Wassers besteht. Dieser Vorgang, der auf der elektrostatischen Anziehung beruht, wird als Hydratation der Ionen (auch Hydration genannt) bezeichnet. An positiv geladene Ionen lagern sich die Wasserdipole mit ihrem negativen Ende, an negativ geladene Ionen mit ihrem positiven Ende an. Sind an Stelle von Wasser andere Lösungsmittel (z.B. flüssiger Ammoniak) beteiligt, so spricht man von Solvatation. |
|
||||||||||||||||